Decreto 405 REGLAMENTO DE PRODUCTOS PSICOTROPICOS
Promulgacion: 02-NOV-1983 Publicación: 20-FEB-1984
Versión: Última Versión - 07-SEP-2022
Url: https://www.bcn.cl/leychile/navegar?i=13066&f=2022-09-07
Art. 2 N° 1
D.O. 07.12.2015boración de productos farmacéuticos de uso humano.
D.O. 12.07.2004 exportación de dichos productos para el año calendario siguiente, a fin de que ese organismo, sobre la base de la información aportada por el solicitante, determine la cantidad que podrá importar o exportar durante ese período.
SALUD,
N° 1, a) de identificación de la droga o producto;
Las modificaciones introducidas al presente reglamento por el D.S. 365, de Salud, de 1984, rigen, según lo dispone su N° 2, a contar del 1° de abril de 1985.
SALUD,
N° 1, b) de identificación de la droga o producto;
SALUD,
1984,
N° 1, c) Importación y Exportación tendrán una validez de cuatro meses contados desde la fecha de su emisión y la respectiva internación o exportación, según corresponda deberá efectuarse, en todo caso, dentro del plazo máximo de 6 meses contados desde la misma fecha.
D.O. 12.07.2004 cada año, indicando la cantidad de psicotrópicos que se propone extraer, producir, fabricar, fraccionar o preparar durante el año calendario siguiente, la que podrá ser objetada por ese Organismo dentro de los treinta días siguientes a su presentación, vencidos los cuales se entenderá aprobada.
SALUD,
N° 1, d) productos psicotrópicos ingresadas al establecimiento y fechas de sus ingresos;
SALUD,
Art.2°,A) y muestras médicas de benzodiazepinas autorizadas, fabricados por el establecimiento, las fechas de fabricación y los nombres y los domicilios de los destinatarios.
SALUD,
N° 1°, f) ingresadas al establecimiento durante el año anterior y los saldos existentes a la fecha de la comunicación, y
SALUD
Art.2°,A) psicotrópicos extraídos o elaborados durante el mismo período y los saldos existentes a la fecha de la comunicación.
El Artículo 2° del Decreto Supremo N° 923, del Ministerio de Salud, dispuso que las modificaciones introducidas al presente decreto supremo entrarán en vigencia el 1° de abril de 1995.
SALUD,
1°, g) llevar actualizado un Libro de Control de Productos Psicotrópicos, visado por el Instituto de Salud Pública, de Chile, o por el Servicio de Salud a quien se asigne esta función en el que se registrarán en forma separada los siguientes datos, respecto de cada droga o producto psicotrópico, indicando su denominación comercial si ello procediera:
SALUD,
N° 1, h) autorizado la internación, distribución o transferencia en su caso;
SALUD
N° 1, i) producto psicotrópico y número de serie, cuando proceda;
SALUD,Art.
2°, B) benzodiazepinas incluidas en la lista IV de este Reglamento por los decretos supremos N°s. 1506, de 1993 y 1186, de 1994, ambos del Ministerio de Salud, con excepción del Flunitrazepam, Lorazepam y Triazolam, las farmacias podrán optar por el mecanismo previsto en el artículo anterior, o bien, llevar actualizado en el mismo Libro de Control de Productos Psicotrópicos, visado por el Servicio de Salud e indicado en el artículo precedente, en forma separada respecto de cada producto psicotrópico que corresponda a la misma forma farmacéutica, e igual dosis y cantidad de unidades posológicas por envase, los siguientes datos:
SALUD,1994,
Art.1°,1°. no podrán tener una cantidad superior a treinta unidades posológicas, salvo que se trate de envases clínicos.
D.O. 12.07.2004 podrá ser inferior a la sexta parte de la superficie de la cara principal del envase.
SALUD,
N° 1, j) psicotrópicos podrán ser adquiridos por los siguientes establecimientos, con intervención del respectivo Director Técnico del establecimiento o del profesionaldel área de la salud responsable, en los casos de las instituciones de investigación médica o científica:
Salud,1995,
Art.2°, a)
DS 78, SALUD
1985.-y consultorios del Estado;
Nº 1
D.O. 20.04.2011Salas de Procedimiento y Pabellones de Cirugía Menor.
Nº 2
D.O. 19.05.2011de entidades que presten servicios de transporte avanzado de enfermos y de entidades que realicen transporte aéreo de personas enfermas o accidentadas.
Art. 3°
D.O. 25.04.1995 Salud respectivo las recetas cheque a que se refiere el artículo 24 y la copia de las guías de entrega aludidas en el inciso anterior, dentro del plazo que se determine por resolución del Ministro de Salud.
El Art. 4° del DTO 923, Salud, publicado el 25.04.1995, dispuso que la modificación introducida al presente artículo regirá a contar del 1° de julio de 1995.
SALUD,
1984,
N° 1, l) psicotrópicos sólo podrán expenderse al público en farmacias o laboratorios mediante "Receta Cheque" en los casos de los productos contenidos en las Listas II y III o "Receta Médica Retenida", tratándose de los contemplados en la Lista IV, según sea su respectiva condición de venta. Ambos tipos de recetas tendrán los formatos que fije el Ministerio de Salud por Resolución.
Art. 2 N° 2
D.O. 07.12.2015farmacéuticas que contengan tetrahidrocanabinoles (todos los isómeros) podrán expenderse al público en farmacias o laboratorios mediante receta médica retenida con control de existencia.
Art. 1º
D.O. 16.02.2008 encuentren incorporados en las Listas II y III, cuyas drogas y principios activos se presenten en una forma farmacéutica que pueda acreditar que el riesgo de abuso es insignificante o nulo, la autoridad sanitaria podrá determinar o reemplazar su condición de venta a la de "Receta Médica Retenida".
El Art. 2º del DTO 143, Salud, publicado el 16.02.2008, dispuso que la modificación introducida en el presente artículo rige a contar del primer día del mes siguiente al de su publicación, fecha a partir de la cual los interesados podrán presentar sus solicitudes ante el Instituto de Salud Pública.
Art. 1 N°1
D.O. 24.05.2017talonarios que los Servicios de Salud proporcionarán a los médicos cirujanos, previa acreditación de su calidad profesional. En ellos deberá individualizarse el nombre y cédula de identidad del médico cirujano.
SALUD, 1984,
N° 1, ll) uno o más formularios, el profesional deberá dar aviso de inmediato a la Dirección del respectivo Servicio de Salud, la que, a su vez, formulará la denuncia correspondiente a la Justicia y lo comunicará a los demás Servicios de Salud. El médico cirujano podrá hacer esta denuncia y deberá, además, publicar el hecho en un aviso destacado en el diario de mayor circulación de la localidad durante tres días consecutivos, y acompañar el recibo de pago de estas publicaciones al solicitar un nuevo talonario de recetas cheques.
SALUD,
1984,
N° 1, m) profesional deberá hacer entrega de ellas al Servicio de Salud correspondiente, al momento de solicitar un nuevo talonario.
SALUD,
1984,
N° 1, n) deberán ser extendidas íntegramente por el médico cirujano y en ellas se anotarán en forma clara y completa los antecedentes indicados en el respectivo formulario, sin dejar espacios en blanco ni enmendaduras. En caso de ser el Decreto 58, SALUD
Art. tercero I a) y b)
D.O. 07.05.2020paciente menor de edad y no tener cédula de identidad, el médico dejará el espacio correspondiente al número de la cédula en blanco y consignará junto al nombre del menor y entre paréntesis, la edad del mismo, en años cumplidos.
SALUD,
1985.-duplicado y el profesional que lo haga registrará en el talón correspondiente los datos que en él se indican.
SALUD,
N° 1 a)
D.O. 30.11.1994 prescripción no podrá superar los 30 días de tratamiento, de acuerdo a la dosificación diaria prescrita, debiendo dispensarse el total de la receta de una sola vez.
El N° 2 del Decreto 2654, Salud, publicado el 30.11.1994, dispuso que vigencia a contar del día 1° del mes siguiente al de su publicación.
SALUD,
1984,
N° 1, ñ) establecimiento y no podrá ser transferido ni cedido a ningún título.
SALUD,
1984,
N° 1, o) y p) médicas retiradas en que se prescriban drogas o productos psicotrópicos deberán ser despachadas personalmente por el Director Técnico de la farmacia o laboratorio de producción, siempre que ellas se presenten por una persona mayor de dieciocho años de edad quien deberá exhibir su cédula de identidad.
SALUD,
1984,
N° 1 q) el Director Técnico anotará, en el espacio destinado a su uso exclusivo, los datos que indica el formulario.
Nº 1 r)
D.O. 23.02.1985 oficinales que contengan drogas de las Listas II y III sólo podrán extenderse y despacharse mediante "receta cheque" y las que contengan drogas de la Lista IV, a través de "receta retenida".
Nº 1 A)
D.O. 28.04.2006 de las cantidades y condiciones que a continuación se indica y que corresponden a una formulación de liberación convencional:
D.O. 03.04.2000
Nº 1 A)
D.O. 28.04.2006
SALUD,
1984,
N° 1, r) receta cheque, las prescripciones de productos psicotrópicos que se formulen en recetarios especiales autorizados para estos efectos por los Servicios de Salud, en los establecimientos asistenciales dependientes del Sistema Nacional de Servicios de Salud, de las Fuerzas Armadas y Carabineros, y de las Universidades y en hospitales y clínicas particulares, destinadas exclusivamente al uso interno de estos establecimientos.
Art. 2
D.O. 05.12.2015cirujanos dentistas podrán prescribir preparados psicotrópicos de la lista IV. Además, podrán adquirir en farmacias dichos preparados, en una cantidad no superior a 150 unidades posológicas, para administrarlos directamente a sus pacientes. En este caso, el expendio de estos productos deberá efectuarse directamente a la persona de estos profesionales, mediante el uso de recetas de su propiedad, las cuales deberán indicar que el expendio se solicita para el uso no personal sino para el ejercicio de su profesión en terceros a los que presta servicios, quedando dichas recetas retenidas, previa individualización del profesional, y registrada en el libro al que alude el artículo 18º de este reglamento, registro que se dispondrá en una sección especial destinada a estas inscripciones.
Salud,1995,
Art.2°, b) productos de la lista IV podrán prescribirlos mediante las correspondientes recetas retenidas, las que sin perjuicio de ajustarse a lo dispuesto en los artículos 23 y 25 de este reglamento, deberán además consignar su uso veterinario y el nombre y cédula de identidad del dueño o responsable del animal al que se efectúa la prescripción.
SALUD,
N° 1,r) muestras médicas de ninguno de los productos psicotrópicos comprendidos en las Listas II, III y IV del Título V, ni efectuar promoción o difusión comercial de ellos, salvo que contenga dosis mínimas de productosDS 406,SALUD
1990, N° 2,
a) psicotrópicos y el Instituto de Salud Pública de Chile autorice específicamente distribuir muestras médicas y promover esos medicamentos.
SALUD, Art.
2°, C) en el artículo anterior, los laboratorios de producción podrán elaborar y distribuir muestras médicas de benzodiazepinas, a excepción de aquellas que contengan lorazepam, triazolam y fluritrazepam, para lo cual deberán declarar, en la solicitud que se presente al Instituto, de conformidad a lo dispuesto en el artículo 16, la cantidad de materia prima que destinarán a su elaboración.
farmacéuticos, y los importen como productos terminados, SALUD, 1° a granel para su fraccionamiento y envase por terceros o materias primas para su fabricación por terceros, podrán entregar muestras médicas de benzodiazepinas, con exceción de aquellos que contengan lorazepan, triazolan y flunitrazepan. Para ello deberán declararlo así, en los documentos a que se refieren los artículos 8° y 9° de este Reglamento, indicando la cantidad del producto terminado, a granel o materia prima que se destinará a muestra médica.
SALUD, 2° dentistas, se materializará mediante recibo que se otorgará en copia y original cuyo formato y contenido será aprobado por resolución del Ministerio de Salud.
SALUD, 2° desde su recepción y estará a disposición de la autoridad sanitaria. La copia quedará en poder del profesional.
SALUD, 2° de estos productos, en forma directa y personalizada, a los profesionales encargados de su prescripción y dispensación.
D.O. 12.07.2004 benzodiazepinas, con excepción de aquellas que contengan lorazepan, triazolam o flumitrazepan, será aplicable también el producto zolpidem.
SALUD,
1984,
N° 1, r) para mantener existencias de productos psicotrópicos deberán conservarlos permanentemente bajo llave y adoptar las demás medidas necesarias para prevenir su hurto, robo, sustracción o extravío.
SALUD,
1984, N° 1,
r) presente reglamento será sancionada por la autoridad sanitaria competente en la forma y con arreglo a los procedimientos previstos en el Libro X del Código Sanitario, sin perjuicio de la responsabilidad penal que pudiera derivar del mismo hecho y de lo establecido en el artículo 3° de la ley 18.164.
r)
D.O. 23.02.1985 sesenta días después de su publicación en el Diario Oficial, fecha en que quedará derogado el decreto supremo 4, de 2 de enero de 1970, del Ministerio de Salud y sus modificaciones, así como toda otra norma, resolución o disposición reglamentaria o administrativa que sea contraria o incompatible con las de este reglamento, tales como las resoluciones 90, de 4 de febrero de 1970; 422, de 20 de mayo de 1971; 7.565, de 27 de noviembre de 1972; 124, de 7 de enero de 1976; 1.324, de 3 de octubre de 1977, todas del Director General de ex Servicio Nacional de Salud, y la 1.707, de 21 de septiembre de 1982, del Director del Instituto de Salud Pública de Chile.
Art. 1
D.O. 18.05.2021
Nº 1
D.O. 25.02.1988 dl-2,5-dimetoxi-
Nº 2 a y c)
D.O. 19.02.1990 2,5-Dimetoxi-4-br
N° 2, Nº 5°
D.O. 12.07.2004 -metil-4-metiltiofe
Art. 1
D.O. 07.12.2015 o 1-(3-clorofenil)
Art. 1
D.O. 28.11.2015 o
Art. 1 N° 1
D.O. 19.11.2020)
 .
.Nº 1
D.O. 19.02.1990 derivadas de la feniletilamina y dimetiltriptamina con efecto alucinógenos contenidas en todo material o preparación, en cualquier cantidad de sustancias, sales, isómeros o mezclas que se indican a continuación:
Art. único N° 1
D.O. 07.09.2022dimetoxifeniletil)-N-(2-metoxibencil)acetamida, (N-ACETIL-25I-NBOMe).
Art. 1 N° 1
D.O. 19.11.2020)
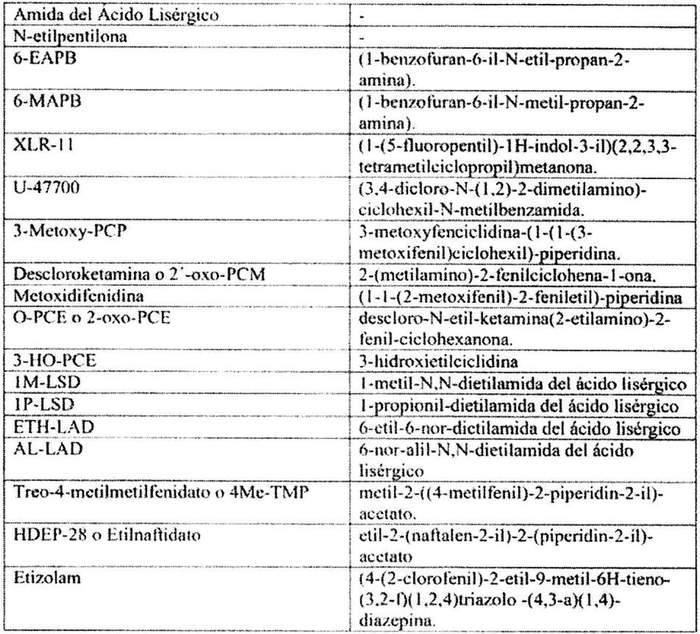 .
. .
.Art. 1, 1)
D.O. 29.06.2021 - BINACA: methyl (2S) – 2 – {[1 -
Art. 1° N° 1
D.O. 08.07.2021: 4-metilaliloxi-3,5-
Art. 1°
D.O. 25.11.2021 - NN- DIMETIL-3,4-
Art. ÚNICO
D.O. 06.01.2022
Art. 1°
D.O. 10.03.2022Etil Heptedrona 2- (etilamino) -1-fenylheptan-1-ona
Nº 1
D.O. 25.02.1988 d-treo-2-amino-1-
Nº 2 b)
D.O. 23.02.1990
Nº 1
D.O. 04.07.1991
N° 2, Nº 5°
D.O. 12.07.2004indol-5-ol
Nº 1 B)
D.O. 28.04.2006noico)
Art. 1 N° 2
D.O. 19.11.2020
 iclohexan-1-ona.
iclohexan-1-ona. Nº 2, d)
D.O. 19.02.1990arbitúrico
Nº 2 c)
D.O. 23.02.1990-ol
ART. 1° Nº 3
D.O. 30.09.1993: Lista IV
Art. 1 Nº 2
D.O. 14.06.1994úrico
N° 2, Nº 5°
D.O. 12.07.2004 - 2 - tiona
El inciso segundo del Artículo 3° del D.S. N° 1.506, del Ministerio de Salud, publicado en el "Diario Oficial" de 30 de septiembre de 1993, dispuso lo que sigue: "Con todo, la incorporación de las siguientes benzodiazepinas a la Lista IV del Título V del Reglamento de Productos Psicotrópicos, decreto supremo N°405 de 1983, de este Ministerio de Salud, regirá a contar de la mencionada fecha, para el solo efecto de su control de importación, exportación, tránsito, producción, fabricación, fraccionamiento, preparación, distribución, transporte y transferencia. Para efectos del control de su expendio, posesión, tenencia y uso regirá 18 meses después de su publicación en el Diario Oficial:
ALPRAZOLAM 8-cloro-1-metil-6-feni-4H-s-triazolo
[4,3-a] [1,4] benzodiacepina
BROMAZEPAM 7-bromo-1,3-dihidro-5-(2-piridil)-
2H-1,4-benzodiacepin-2-ona
CAMAZEPAM 7-cloro-1,3-dihidro-3-hidroxi-1-
metil-5-fenil-2H-1,4-benzodiacepin-2
-ona dimetilcarbamato (éster)
CLOBAZAM 7-cloro-1-metil-5-fenil-1H-1,5-
benzodiacepin-2,4(3H,5H)-diona
CLONAZEPAM 5-(o-clorofenil)-1,3-dihidro-7-nitro
-2H-1,4-benzodiacepin-2-ona
CLORAZEPATO 7-cloro-2,3-dihidro-2-oxo-5-fenil-
1H-1,4-benzodiacepin-3-ácido
carboxílico
CLORDIAZEPOXIDO 7-cloro-2-(metilamino)-5-fenil-3H-
1,4-benzodiacepin-4-óxido
CLOTIAZEPAM 5-(o-clorofenil)-7-etil-1,3-dihidro-
1-metil-2H-tieno[2,3-e]-1,4-diacepin
-2-ona
CLOXAZOLAM 10-cloro-11b-(o-clorofeni)-2,3,7,11b
-tetrahidrooxazolo [3,2d][1,4]
benzodiacepin-6(5H)-ona
DELORAZEPAM 7-cloro-5-(o-clorofenil)-1,3-dihidro
-2H-1,4-benzodiacepin-2-ona
DIAZEPAM 7-cloro-1,3-dihidro-1-metil-5-fenil-
2H-1,4-benzodiacepin-2-ona
ESTAZOLAM 8-cloro-6-fenil-4H-s-triazolo[4,3-a]
[1,4] benzodiacepina
FLUDIAZEPAM 7-cloro-5-(o-fluorofenil)-1,3-
dihidro-1-metil-2H-1,4-benzodiacepin
-2-ona
FLURAZEPAM 7-cloro-1-[2-(dietilamino)etil]-5-(o
-fluorofenil)-1,3-dihidro-2H-1,4-
benzodiacepin-2-ona
HALAZEPAN 7-cloro-1,3-dihidro-5-fenil-2,2,2-
trifluoroetil)-2H-1,4-benzodiacepin-
2-ona
HALOXAZOLAM 10-bromo-11b-(o-fluorofenil)-2 ,3,
7, 11b-tetrahidrooxazolo[3,2-d][1,4]
benzodiacepin-6(5H)-ona
KETAZOLAM 11-cloro-8,12b-dihidro-2,8-dimetil-
12b-fenil-4H-[1,3]-oxazino[3,2-d]
[1,4]benzodiacepin-4,7(6H)-diona
LOFLAZEPATO DE
ETILO etil 7-cloro-5-(o-fluorofenil)-2,3-
dihidro-2-oxo-1H-1,4-benzodiacepin-
3-carboxilato
LOPRAZOLAM 6-(o-clorofenil)-2,4-dihidro-2-[(4-
metil-1-piperacinil)metileno]-8-
nitro-1H-imidazo[1,2-a][1,4]
benciodiacepin-1-ona
LORMETAZEPAM 7-cloro-5-(o-clorofenil)-1,3-dihidro
-3-hidroxi-1-metil-2H-1,4-
benzodiacepin-2-ona
MEDAZEPAM 7-cloro-2,3-dihidro-1-metil-5-fenil-
1H-1,4-benzodiacepina
MIDAZOLAM 8-cloro-6-(o-fluorofenil)-1-metil-4H
-imidazo[1,5-a] benzodiacepina
NIMETAZEPAM 1,3-dihidro-1-metil-7-nitro-5-fenil-
2H-1,4-benzodiacepin-2-ona
NITRAZEPAM 1,3-dihidro-7-nitro-5-fenil-2H-1,4-
benzodiacepin-2-ona
NORDAZEPAM 7-cloro-1,3-dihidro-5-fenil-2H-1,4-
benzodiacepin-2-ona
OXAZEPAM 7-cloro-1,3-dihidro-3-hidroxi-5-
fenil-2H-1,4-benzodiacepin-2-ona
OXAZOLAM 10-cloro 2,3,7,11b-tetrahidro-2-
metil-11b-fenitoxazolo [3,2-d][1,4]
benzodiacepin-6(5H)-ona
PINAZEPAM 7-cloro-1,3-dihidro-5-fenil-1-(2-
propinil)-2H-1,4-benzociacepin-2-ona
PRAZEPAM 7-cloro-1-(cliclopropilmetil)-1,3-
dihidro-5-fenil-2H-1,4-benzodiacepin
-2-ona
TEMAZEPAM 7-cloro-1,3-dihidro-3-hidroxi-1-
metil-5-fenil-2H-1,4-benzodiacepin-
2-ona
TETRAZEPAM 7-cloro-5-(1-ciclohexen-1-il)-1,3-
dihidro-1-metil-2H-1,4-benzodiacepin
-2-ona"."
El Artículo 2° del Decreto Supremo N° 1.186, del Ministerio de Salud, publicado en el 14 de Junio de 1994, dispuso que las modificaciones introducidas al presente decreto supremo comenzarán a regir a contar de la fecha de su publicación en el Diario Oficial. Con todo, la incorporación de las substancias a que se refiere su N° 2, regirá a contar de esa fecha, para el solo efecto de su control de importación, exportación, tránsito, producción, fabricación, fraccionamiento, preparación, distribución, transporte y transferencia. Para efectos de su control de expendio, posesión, tenencia y uso regirá a contar del 30 de abril de 1995.
